New Therapeutic Target in the Fight Against ALS
Scientists uncover a new protein in a pathway for neurotoxicity and cell death
A new study published in Nature takes us one step forward in understanding the key mechanisms behind neurodegenerative diseases. With the urgent need for human cellular models to study such pathologies, scientists have developed a new 2D cell culture model with features mirroring those of human brains, with the support from MaxWell Biosystems’ High-Density Microelectrode Arrays (HD-MEAs). Delving deeper into the effects of the abnormal accumulation of TAR DNA-binding protein 43 (TDP-43), involved in diseases like amyotrophic lateral sclerosis (ALS), scientists identified a new player – a protein called neuronal pentraxin 2 (NPTX2) – that teams up with TDP-43 to induce neurotoxic effects and presents a potential therapeutic target.
This groundbreaking work, entitled “A model of human neural networks reveals NPTX2 pathology in ALS and FTLD” was led by Dr. Marian Hruska-Plochan in Prof. Dr. Magdalini Polymenidou‘s lab at the Department of Quantitative Biomedicine, University of Zurich, Switzerland.

The study was done in collaboration with the Department of Biosystems Science and Engineering, ETH Zürich; the Department of Molecular Life Sciences, SIB Swiss Institute of Bioinformatics, Brain Research Institute, and Institute of Neuropathology, from the University of Zurich; the Masaryk University Brno, Czech Republic; UCL Institute of Neurology, UK; and the University of Bern, NCCR RNA and Disease Technology Platform, Switzerland.
MaxWell Biosystems’ HD-MEA technology was utilized in the functional characterization of the induced pluripotent stem cell (iPSC)-derived neuronal cell lines developed in this work. With the high resolution and high data quality provided by these HD-MEAs, it was possible to extract the activity of these neurons in unprecedented detail, accessing network, cellular and subcellular features. These results significantly contributed to confirming the electrophysiological activity of these neurons, reaveling developed interconnected networks and coordinated firing.
“MaxOne HD-MEAs allowed us to perform multiple recordings simultaneously and later we were able to analyze not only network properties from the neurons but single cell metrics”, Dr. Hruska-Plochan highlighted.
The challenge of studying TDP-43 pathologies
Why TDP-43 and how is it related to neurodegenerative diseases?
TDP-43 is an RNA-binding protein that accumulates in neurons from patients with neurodegenerative diseases, including amyotrophic lateral sclerosis (ALS) and frontotemporal lobar dementia (FTLD), with patients suffering from severe movement and cognitive impairments. In healthy cells, TDP-43 is mainly located in the nucleus, where it regulates the processing of hundreds of RNA targets. In diseased cells, TDP-43 forms toxic aggregates, leading to the loss of its normal function, affecting its RNA targets and consequently disturbing cellular function.
Human-specific mechanisms related to TDP-43-induced pathologies cannot be directly studied in animal models. This highlights the need for human cellular models of neurodegeneration that are reproducible and stable in vitro. Such models can help scientist figure out what causes the diseases and how they progress, key for therapy development.
What challenges are scientists facing?
In recent years, iPSC-derived models have been developed with the goal of understanding neurodegenerative diseases. However, studies with iPSC-derived neurons from patients with TDP-43 dysregulation have shown little to no TDP-43 pathology, possibly due to an early maturation state of the cultured neurons.
In an effort to address this challenge, Dr. Hruska-Plochan and colleagues developed a new stem cell model capable of giving rise to functional neuronal networks. They used this model to investigate TDP-43 pathologies, uncovering a new pathway of neurotoxicity and opening the door for a potential therapeutic target.
Generating a new human cellular model
How was the new cellular model developed?
First, the authors reprogrammed human skin fibroblasts to derive iPSCs. These iPSCs were manually selected based on their colony morphology. This process generated a neural stem cell line termed as induced colony morphology neural stem cells (iCoMoNSCs), which can differentiate in both neurons and glial cells.
To validate their model, they used used single-cell-RNA sequencing (scRNA seq) to analyze gene expression in individual cells. This technique allows scientists to examine the genetic makeup or transcriptional profile of each cell, disclosing the diversity and complexity of cell populations. Despite lacking a 3D organ-like structure, they found a variety of neuronal and glial cell types, comparable to those found in the human brain and brain organoids – an important feature in a model for studying cellular function, development and disease.
The next step relied on studying how the iCoMoNSCs-derived cells matured and formed synaptic connections. By labelling cells in 3-month-old cultures with specific markers, the authors identified neurons, glial cells, and synaptic structures. Additionally, transmission electron microscopy showed a typical synaptic morphology. However, one question remained – are these cells functionally active?
Two-photon calcium imaging was performed, revealing sparse spontaneous activity patterns. To further confirm such activity, the authors conducted whole-cell patch clamp experiments, where they observed iCoMoNSC-derived neurons to contain voltage-dependent channels and to be electrophysiologically active.
HD-MEAs unravel functional features
But did the neurons mature and develop interconnected networks? Are they firing together?
To answer these questions, the cell cultures were plated onto the MaxOne high-density microelectrode arrays (HD-MEAs) at different time points after differentiation and allowed to reconnect for one month before recordings. Using MaxLab Live software, various metrics, ranging from network to subcellular resolution, were measured to characterize and compare the neuronal cultures at different maturation stages (young, middle, old).
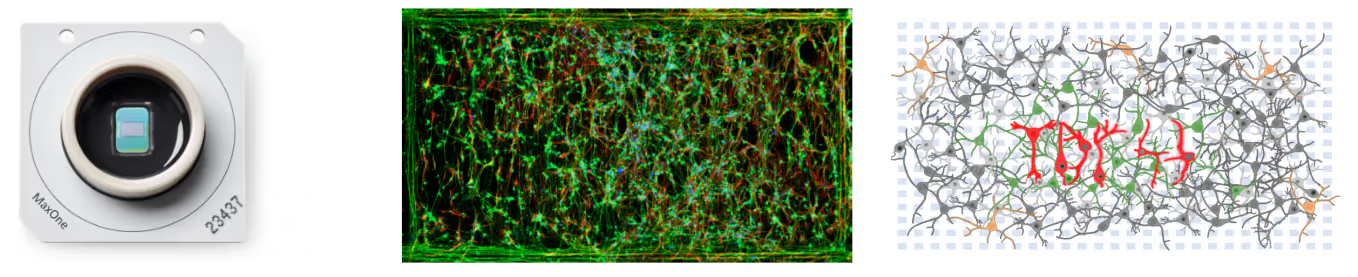
Among the metrics evaluated with MaxOne HD-MEAs, the authors found lower burst activity in young cultures compared to old cultures, along with an increase in spontaneous activity over time and longer branch length across development. Such findings indicated an increased maturation of the aging iCoMoNSC-derived neurons and revealed the formation of functional neuronal networks, which the authors termed as iNets.
TDP-43 overexpression in iNets unravels new RNA targets
With a powerful model in hands, what comes next?
Previous studies have shown that less than 2% of cortical cells from FTLD patients exhibit pathological alterations in TDP-43. To replicate this phenomenon, the authors artificially increased the expression of TDP-43 in iNets using a lentivirus vector. They observed a gradual decrease in the number of the infected neurons, indicating that overexpressing TDP-43 led to its aggregation and fragmentation, proving to be toxic to the neurons.
Using scRNA-seq, the authors identified a distinct transcriptional profile in iNets with TDP-43 overexpression and pathology. Over time, the abnormal levels of TDP-43 led to changes in the expression of many genes. Notably, among these genes were STMN2 and UNC13A, known human-specific RNA targets of TDP-43.
By analyzing previous data from control and FTLD patient brain samples, it was possible to identify the other dysregulated RNAs as TDP-43 binding targets, with the binding in the vast majority altered in FTLD patients.
As similar as for the TDP-43 overexpression in the iNets neurons, the expression of these newly identified RNA targets was also altered in scRNA-seq datasets previously obtained from ALS-FTLD patient brains.
NPTX2 as a new potential therapeutic target for TDP-43 pathologies
Did any of these new RNA targets stand out?
To explore this, the authors compared iNets and patient scRNA-seq datasets. They found neuronal pentraxin 2 (NPTX2) to be the most significantly upregulated RNA, indicating a potential role in TDP-43 pathology. NPTX2 encodes for the synaptic protein NPTX2, and its levels are controlled by TDP-43 binding to the RNA.
Interestingly, overexpressing TDP-43 in the iNets caused an abnormal accumulation of NPTX2. But not only a higher expression of TDP-43 led to this effect – using a lentivirus to knockdown or reduce the expressed levels of TDP-43 also led to an increase in NPTX2 levels. Notably, both results had similarities with the transcriptomic alterations found in the ALS-FTLS patient brains.
The authors did not stop there – they discovered that the harmful effects caused by TDP-43 overexpression were more severe than those caused by increased NPTX2 expression alone. This highlights the role of NPTX2 as one of the downstream contributors of TDP43-driven toxicity. Hence, by using the knockdown technique and correcting NPTX2 levels in iNets overexpressing TDP-43, they were able to rescue cells from TDP-43-induced neurodegeneration.
What is the significance of these findings
This study highlights two significant breakthroughs: the development of a powerful new human cellular model and the discovery of a new player in the toxic pathway leading to neurodegeneration in TDP-43 pathologies.
Given the pressing need for human cellular models to investigate neurodegenerative diseases, the iCoMoNSCs and derived iNets present promising tools for uncovering human-specific characteristics related to these disorders.
They are suitable for studying network connectivity and axon tracking using HD-MEAs. Additionally, their diverse neuronal and glial populations, mirroring those found in the human brain and brain organoids, make them valuable for drug screening and development.
The similarities of transcriptional profiles between the iNets overexpressing TDP-43 and patient brains strengthens their relevance as a human disease model, and their comparison allowed the authors to identify NPXT2 as a protein worth of further exploration.
Overall, the authors propose NPTX2 as a pivotal neuronal target of TDP-43, suggesting that its abnormal increase can lead to a pathological cascade causing neuronal death in ALS/FTLD. NPTX2 emerges as a potential therapeutic target for TDP-43 pathologies, alongside the proteins translated from STMN2 and UNC13A RNAs.
What will come next
This new publication leaves many questions unanswered. As such, the authors emphasize the importance of:
- Using HD-MEAs to study different TDP-43 states in virally manipulated cells and infer on their electrophysiological properties.
- Delving deeper into understanding the molecular mechanisms behind NPTX2 toxic effect in the neurons.
- Exploring the potential collaboration between NPTX2, STMN2, and UNC13A proteins in the harmful pathway that leads to neuronal death in TDP-43 pathologies.
- Experimenting with different methods to correct NPTX2 levels and understanding their impact on TDP-43 pathology.
Related
Resources
MaxOne
Versatility and functionality in one compact device

MaxLab Live
All-in-one Software
Our Technology
Multi-/Micro-electrode Arrays

Disease Modeling

Neuronal Cell Cultures